Из чего состоит вакцина «КовиВак»
«КовиВак» — инактивированная вакцина, разработанная в Федеральном научном центре исследований и разработки иммунобиологических препаратов имени М. П. Чумакова. «Инактивированная» означает, что в основе препарата содержится «убитый» вирус-возбудитель, который потерял возможность заражать клетки. Чтобы инактивировать вирус, в вирусную жидкость добавляют бета-пропиолактон — токсичное вещество, которое используется при производстве всех основных инактивированных вакцин против коронавируса. Это одна из самых старых технологий производства вакцин — с ее помощью, например, создана вакцина от полиомиелита.
Когда вакцина с убитыми вирусными частицами попадает в организм человека, препарат не вызывает заболевание, но иммунитет распознает болезнетворные агенты и вырабатывает антитела.
«Разработка инактивированных вакцин является рентабельной и надежной благодаря долгой и успешной истории ее использования. Несколько инактивированных вакцин против инфекции SARS-CoV-2 разрабатываются во всем мире, и, по крайней мере, пять показали успех в доклинических и клинических испытаниях, что привело к их разрешению для использования», — говорится в статье.
К таким вакцинам относятся, например, китайские препараты Sinovac и Sinopharm.
В феврале 2021 года «КовиВак» зарегистрировал Минздрав — препарат стал третьей зарегистрированной вакциной в России наряду со «Спутником V» и «ЭпиВакКороной». С 28 марта вакцина начала поступать в гражданский оборот.
Что означает первая публикация
Несмотря на то, что вакцина уже зарегистрирована и поставляется в регионы России для вакцинирования населения, о препарате до сих пор не было никаких публикаций в международных рецензируемых изданиях. Статья с данными доклинического исследования — первая, и она получила положительные оценки независимой группы рецензентов.
«Результаты доклинического исследования опубликованы в достаточно хорошем рецензируемом издании — это означает, что они оценены независимой группой рецензентов и оценка вынесена положительная. Действительно, ознакомление со статьей дает представление о скрупулезном доклиническом исследовании прежде всего безопасности вакцины, но также и ее иммуногенности (способности стимулировать выработку антител)», — поясняет Оксана Станевич.
Тем не менее пока ученые опубликовали лишь результаты доклинических исследований на животных — соответственно, о безопасности вакцины для людей судить по этой публикации однозначно нельзя.
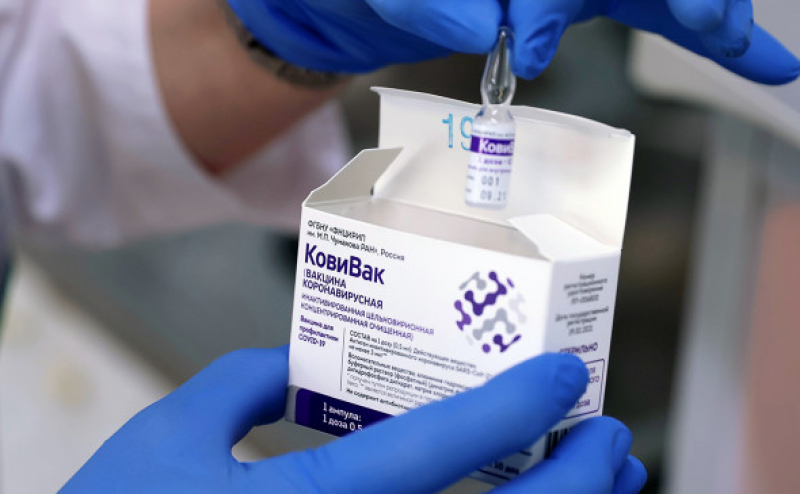
Вакцина «КовиВак». Фото: Виталий Белоусов / РИА Новости
https://www.rbc.ru/society/01/06/2021/60af6de69a794740bb5b5b92
Фото: Виталий Белоусов / РИА Новости
Подробнее на РБК:
https://www.rbc.ru/society/01/06/2021/60af6de69a794740bb5b5b92
Как проводились исследования
Ученые больше года проводили эксперименты с безопасностью вакцины у животных. Исследователи наблюдали за состоянием морских свинок, мышей, сирийских хомяков и мартышек, получивших вакцину, а затем сравнивали уровень их иммунного ответа и безопасность вакцины с контрольной группой.
Всего в исследовании участвовали 20 морских свинок и 25 мышей, которым ввели вакцину, и аналогичное количество животных, получивших физраствор. Исследователи наблюдали за ними в течение недели и в итоге не выявили никаких патологических изменений у тех, кто получил вакцину.
Кроме того, ученые пришли к выводу, что «КовиВак» не токсичен, даже если препарат вводить многократно и в большой дозировке. Вакцину вводили мышам и морским свинкам ежедневно в течение 10 суток — подобная дозировка не повлияла на их здоровье. Вскрытие также не показало изменений в органах.
Препарат исследовали и на приматах. Четырем самкам и двум самцам ввели вакцину дважды с интервалом в 14 дней. Биохимические анализы крови мартышек были в норме, существенных различий между контрольной и экспериментальной группой ученые не выявили.
Чтобы исключить возможность негативного влияния белков коронавируса на плод, действие «КовиВака» проверили на беременных крысах. Исследователи разделили 60 крыс на три группы. Им вводили вакцину на 2-й, 9-й и 16-й дни беременности, причем одну из групп прививали двойной дозой. Ни признаков интоксикации, ни летального исхода у крыс не наблюдалось. Часть животных в каждой группе умерщвляли на 20-ый день беременности. Вскрытие также не показало никаких патологических изменений органов и самого плода.
За потомством оставшейся половины животных в каждой группе наблюдали после родов в течение 60 дней. Ученые отмечают, что смертность за весь период наблюдения не превышала 4% и не отличалась от смертности в контрольной группе. Вакцинация, как говорится в статье, не вызвала увеличение смертности потомства, а также не повлияла на его развитие.

Оксана Станевич. Фото из личного архива
Насколько вакцина безопасна
Авторы исследования делают вывод, что его результаты доказывают безопасность вакцины для животных. Именно этот факт стал поводом для инициирования исследований у людей.
«Из имеющейся публикации нельзя сделать выводы о нежелательных явлениях вакцины у людей, однако можно сказать, что вакцина не действует на репродуктивную функцию и плод внутриутробно. Отсутствие серьезных нежелательных явлений у мартышек указывает на высокую вероятность их отсутствия у людей», — поясняет Оксана Станевич.
В июне разработчики вакцины получили разрешение Минздрава на проведение третьей фазы клинических исследований. В них принимают участие 32 тыс. человек в возрасте от 18 до 60 лет. Исследования проходят в 17 медицинских центрах Москвы, Петербурга, Кирова, Челябинска, Белгородской, Оренбургской, Курской областей и Татарстана.
Несмотря на то, что клиническое исследование третьей фазы стартовало совсем недавно, «КовиВаком» уже прививают — причем за вакциной выстраиваются очереди и она быстро заканчивается.
«Разные фазы клинического исследования проводились параллельно, и на самом деле результаты 1/2 фазы и частично 3 фазы клинического исследования уже имеются, просто они пока не опубликованы, ― поясняет Оксана Станевич. ― И хотя мы не видим информацию в виде доступных публикаций, отчеты об этих фазах продемонстрировали безопасность исследований, иначе они были бы приостановлены», — комментирует Оксана Станевич.
По ее словам, ответа на вопрос, стоит ли прививаться этой вакциной, в появившейся публикации нет. Тем не менее, сам факт наличия такой публикации говорит о том, что доклиническое исследование вакцины проведено должным образом, и она точно могла быть допущена к исследованию на людях.