Расскажите, каков основной фокус работы?
В опубликованном обзоре мы фокусируемся на диэлектрических свойствах биологических тканей, растворов и жидкостей в контексте терагерцовой биофотоники. Его цель – привлечь внимание сообщества квантовой электроники к важности разработки диэлектрических моделей водосодержащих сред в диапазоне терагерцовых частот. Кроме того, мы попытались определить основные тенденции использования терагерцового излучения в биологических и медицинских исследованиях, где вода является основным объектом.
Мы рассматривали воду, потому что она играет ключевую роль в формировании и стабилизации биосистем, является универсальным маркером их состояния и функционирования. Именно диэлектрические свойства воды составляют основу диагностических методов, поэтому мы начали наш обзор с анализа физических моделей, описывающих сложную диэлектрическую проницаемость жидкой воды и водосодержащих сред в диапазоне терагерцовых частот.
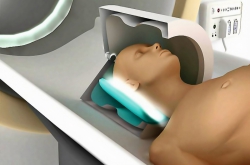
В статье мы обсуждаем современные приборы и методы ТГц-спектроскопии и визуализации, которые широко применяются в ТГц-биофотонике. Такие разработки позволяют визуализировать компоненты тканей: клетки, микрофибриллы и даже клеточные органеллы. Мы также собрали информацию о современных технологиях доставки терагерцового излучения в труднодоступные ткани и внутренние органы и рассмотрели новые методы анализа терагерцовых спектров, основанные на машинном обучении, распознавании образов, химической визуализации и выявлении пространственного распределения различных веществ в ткани.
Почему, несмотря на высокое поглощение в тканях, терагерцовое излучение интересно для применений в биологических объектах и какими эти применения могут быть?
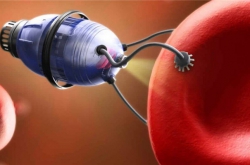
Молекулу воды можно рассматривать как универсальный маркер терагерцового диапазона частот, поэтому терагерцовое излучение чувствительно к различным процессам, происходящим в живых тканях и клетках. Высокая чувствительность терагерцовых волн к содержанию воды и ее состоянию в тканях позволяет применять технологии на основе этого излучения в диагностике злокачественных новообразований, уделяя особое внимание контрасту изображения, наблюдаемого между здоровыми и патологическими тканями.

В статье мы также рассматриваем недавние применения терагерцовой отражательной спектроскопии для измерения слезной пленки роговицы глаза человека при заболеваниях «сухого глаза». Результаты этих исследований показывают потенциал подобных технологий для офтальмологии. Другими медицинскими применениями терагерцового излучения могут быть диагностика ожоговых ран и патологических изменений крови или кожи пациентов с диабетическими осложнениями, а также ряд других заболеваний.
В чем преимущества таких методов по сравнению с аналогами?
Другие современные диагностические методы не могут определить, является ли определенное новообразование опухолью, и если да, то доброкачественная она или злокачественная. Они имеют ограниченные возможности оценки начального размера патологического развития ткани и диагностики процесса заживления. Такие приборы могут быть даже опасны из-за вредного для здоровья ионизирующего излучения.
Есть ли у применения терагерцового излучения в биообъектах какие-либо риски?
Основной риск таких методов ассоциируется с теплом, поэтому в обзоре представлена тепловая модель взаимодействия терагерцового излучения с тканями. Результат численного моделирования показывает, что облучение тканей со средней мощностью 100 мкВт, 10 мВт, 100 мВт и 300 мВт может вызвать нагрев объекта на 0,004, 0,43, 4,32 и 12,95 градусов соответственно. Таким образом, повышение температуры ткани заметно, когда мощность достигает нескольких милливатт. Однако мощность выходного излучения ТГц-спектроскопии и связанных с ней методов диагностики и визуализации не превышает несколько милливатт, поэтому тепловых или нелинейных эффектов в исследуемом объекте не ожидается.
Другим ограничением подобных методов считается сильное поглощение ТГц-волн молекулами воды. Оно не позволяет волнам проникать в гидратированные ткани и вызывать терагерцовый отклик. Но эти эффекты можно обойти. Например, в статье мы рассказали о новых подходах на основе замораживания тканей «ex vivo», а также об оптическом просветлении тканей с помощью специальных жидких агентов.
Как появилась идея такой работы и сколько заняла ее реализация?
Идея появилась примерно полтора года назад. Мы выиграли российский грант РФФИ (КОМФИ), который объединил коллективы четырех терагерцовых лабораторий из разных городов России, среди которых Москва (МГУ), Томск (ТГУ), Санкт-Петербург (Университет ИТМО) и Нижний Новгород (ИФМ РАН). Руководителем проекта стал профессор Александр Павлович Шкуринов. Суть всего проекта заключается в исследовании биологических тканей, жидкостей и выдыхаемого воздуха на признаки социально-значимых заболеваний в терагерцовом диапазоне частот.
Я предложила написать совместную обзорную статью, а Александр Павлович поддержал мою инициативу и пригласил в эту работу иностранных коллег из Франции, Южной Кореи, Израиля и Австралии. Один из соавторов, профессор Валерий Викторович Тучин, получил письмо-поддержку от очень известного журнала Progress in Quantum Electronics.

В начале 2018 года РФФИ объявил конкурс совместных проектов Россия-Франция и мы переключились с нашими французскими соавторами на написание этой конкурсной заявки. В результате мы выиграли несколько проектов, в том числе я выиграла грант совместно с лабораторией IMS Университета Бордо. В мае я провела две недели в этой лаборатории, занимаясь и этой статьей, и научными исследованиями. 3 июля профессор Шкуринов собрал нас в Париже на совместную российско-французскую встречу, где мы обсуждали нашу статью и научные задачи по выигранным грантам. Поэтому можно сказать, что написание статьи было очень захватывающим и при этом последовательным процессом, в центре которого мне было крайне интересно находиться.