Как диагностируют и лечат рак сегодня
Сегодня для лечения злокачественных опухолей в основном применяют лучевую терапию и химиотерапию. Но у каждого из этих методов есть свои недостатки. При использовании радиотерапии, когда врачи облучают опухоль, часто повреждаются и окружающие опухоль здоровые ткани. При химиотерапии пациенту внутривенно вводят специальные лекарственные препараты, которые токсичны для активно делящихся клеток. Но к таким клеткам относятся не только опухолевые, но и здоровые клетки и ткани организма. Поэтому побочные эффекты химиотерапии часто проявляются в тех тканях, клетки которых быстрее обновляются — из-за этого, например, выпадают волосы и ломаются ногти.
С методами диагностики рака тоже связан ряд проблем. Например, при использовании магнитно-резонансной томографии может не хватать контрастности изображения. Это связано с тем, что на начальных этапах заболевания метастазы опухоли могут быть слишком малы, чтобы разглядеть их без специальных контрастных агентов. Существующие же агенты не всегда достаточно эффективны, а также оказывают токсичное воздействие на организм.
Другой подход к лечению и диагностике рака — создание узконаправленных наночастиц. Однако область их применения, как правило, ограничена — для каждого метода лечения и диагностики (например, для магнитной гипертермии, МРТ, КТ и других) нужно создавать отдельные частицы. При этом вводить в организм сразу несколько частиц нельзя, так как это может еще больше подорвать здоровье пациента. Поэтому во время лечения врачам приходится выбирать какую-то одну конкретную частицу или агент. Если же она не даст прогресса в лечении, применять следующую, но делать это можно только спустя определенное время. В итоге все это растягивает лечение и, в свою очередь, также снижает его общую эффективность.
Команда SCAMT. Фото: Дмитрий Григорьев / ITMO.NEWS
Что сделали ученые ИТМО
Чтобы решить эти проблемы, ученые ИТМО попытались объединить в своей разработке сразу несколько методов терапии и диагностики рака ― радиотерапию, магнитную гипертермию и МРТ. В результате исследователи создали универсальную магнитную частицу из феррита цинка и феррита марганца, которая сможет одновременно выполнять несколько задач: применяться для диагностики в МРТ, а также выступать в качестве агента для магнитной гипертермии и ретранслятора для лучевой терапии. Это позволит обеспечить последовательный, комплексный и безопасный подход к диагностике и лечению рака.
В статье, опубликованной в Journal of Materials Chemistry B, ученые показали, что разработанные наночастицы могут выступать контрастными агентами. При этом частицы работают в двух самых распространенных клинических режимах установки, при которых можно обнаружить патологии, — Т1 и Т2. Как отмечают авторы разработки, такая бимодальность позволяет получить больше информации при диагностике. Для изучения контрастных свойств частиц ученые подготовили специальный водный раствор с наночастицами и проверили их на клиническом аппарате МРТ.
Еще один потенциальный способ применения полученных наночастиц — лечение рака. Чтобы проверить, как работает радиотерапия с использованием наночастиц, их инкубировали вместе с раковыми клетками толстой кишки человека в течение суток в чашке Петри. После этого клетки подвергали разным дозам рентгеновского излучения и изучали выживаемость клеток в течение определенных интервалов времени. Оказалось, что наночастицы лучше всего уничтожают раковые клетки при низких дозах облучения — эффективность в этом случае выросла примерно на 40%.
Слева: исследование выживаемости клеток в присутствии наночастиц в зависимости от их концентрации Справа: анализ на поглощение клетками наночастиц. Источник: pubs.rsc.org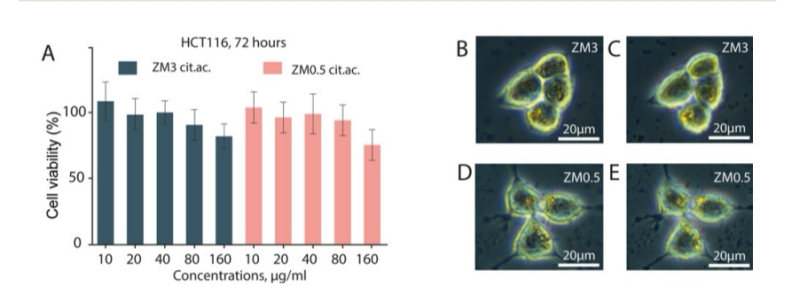
Кроме того, как показали исследования ученых, наночастицы могут разогреваться во внешнем магнитном поле — благодаря этому их можно использовать и при магнитной гипертермии. Это метод лечения, при котором магнитные наночастицы нагревают за счет переменного магнитного поля до 42 градусов за несколько секунд. При такой температуре раковые клетки уже погибают (так как у их белков разрушается структура), а здоровые ― все еще остаются живыми. Гипертермия позволяет достичь большей селективности лечения ― за счет того, что врачи могут воздействовать только на конкретные ткани.
На изображении представлены основные этапы разработки композитных наночастиц. На первом этапе с помощью двухстадийного гидротермального синтеза были получены магнитные наночастицы со структурой ядро-оболочка. На втором их проанализировали на способность проявлять контрастные свойства, разогреваться во внешнем магнитном поле и усиливать ренгеновское излучение для последовательной диагностики и терапии. Источник: pubs.rsc.org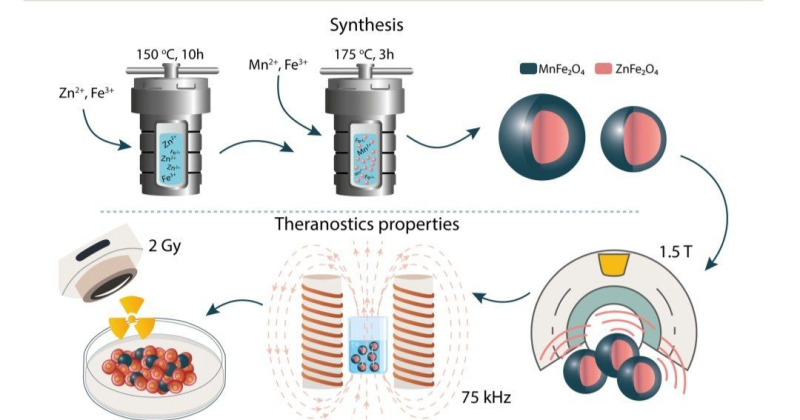
Как создавали наночастицу
Наночастица состоит из двух компонентов: ядро сделано из феррита цинка, а оболочка — из феррита марганца. Это простые и удобные в синтезе материалы, которые имеют приемлемые показатели цитотоксичности. Кроме того, ферриты обладают суперпарамагнитными свойствами, за счет которых наночастицы на их основе можно использовать в МРТ и в магнитной гипертермии.
По сути, наночастицу собирали из молекул — для этого использовали гидротермальный синтез. Принцип его работы напоминает работу пароварки: химические элементы вносят в среду с повышенными температурой и давлением, в результате чего получаются экстремальные условия, в которых протекает синтез частиц.
Ученые охарактеризовали полученные частицы с точки зрения химического состава, структуры, размера, а также проверили их на цитотоксичность — совместимость с живыми клетками.
Перспективы
«Мы уже доказали, что наши частицы могут совмещать в себе как диагностические свойства для МРТ, так и терапевтические за счет магнитной гипертермии и радиотерапии — эффект последней удалось увеличить на 40%. Наши частицы можно использовать в Т1 и Т2 режимах работы МРТ — это их достоинство и недостаток одновременно. С одной стороны, это делает частицы универсальными. С другой — чтобы получить максимально четкое и контрастное изображение, нам необходимы специфические частицы для конкретного режима. Поэтому мы обратили внимание на пробел в понимании механизмов и пределов контрастных наночастиц в Т1 МРТ-режиме. В дальнейшем мы планируем разработать и исследовать специфические магнитные наночастицы, настроенные под конкретный режим работы МРТ (Т1)», — рассказал один из авторов исследования, младший научный сотрудник лаборатории прикладных материалов для энергетики Илья Шабалкин.
Илья Шабалкин. Источник: scamt.ifmo.ru
Статья: Ilia Shabalkin, Alexey Komlev, Sergey Tsymbal, Oleg Burmistrov, Vladimir Zverevb, Pavel Krivoshapkin. Multifunctional tunable ZnFe2O4@MnFe2O4 nanoparticles for dual-mode MRI and combined magnetic hyperthermia with radiotherapy treatment (Journal of Materials Chemistry B, 2023).