Бесперебойную работу органов и организма в целом во многом обеспечивает межклеточная коммуникация. Клетки распределяют питательные вещества, участвуют в их синтезе и транспорте, помогают удалять токсины и защищают от инфекций. При нарушении межклеточной коммуникации восстановление мышц и костей затрудняется. Также могут развиться различные заболевания, например болезнь Альцгеймера. Чтобы иметь возможность исправить это, нужно досконально понимать механизм взаимодействия клеток между собой.
Один из механизмов передачи сигнала от клетки к клетке — ионные токи. Это движение ионов натрия, калия и кальция сквозь мембрану клетки во внеклеточное пространство и обратно внутрь клетки. Каждый тип ионов отвечает за конкретную функцию: катионы натрия проводят нервный импульс, катионы калия регулируют мембранный потенциал клетки, а катионы кальция помогают сокращать мышцы. Допустим, человек ощущает боль или стресс — в ответ в его организме выделяется вещество, которое инициирует реакцию в клетке. Например, норэпинефрин (молекула адреналина) активирует в клетке IP3 ионные каналы, и клетка высвобождает ионы кальция, при этом сокращаясь и передавая сигнал своим «соседям». Дальше как в эффекте домино: постепенно клетки сокращаются, а затем — и мышцы.
Для изучения ионных токов используют несколько типов систем. Один из них построен на прокалывании клетки микроэлектродом, но такое влияние может спровоцировать выброс специфических белков, которые будут мешать измерениям. Для других типов выращивают клеточную ткань, где искусственно делают разрыв — но и здесь есть вероятность повреждения клетки. Ученые научно-образовательного центра инфохимии ИТМО создали биосовместимую систему для обнаружения ионных токов во внеклеточном пространстве. Она позволяет следить за клетками в естественной среде обитания, не вмешиваясь в их жизнедеятельность.
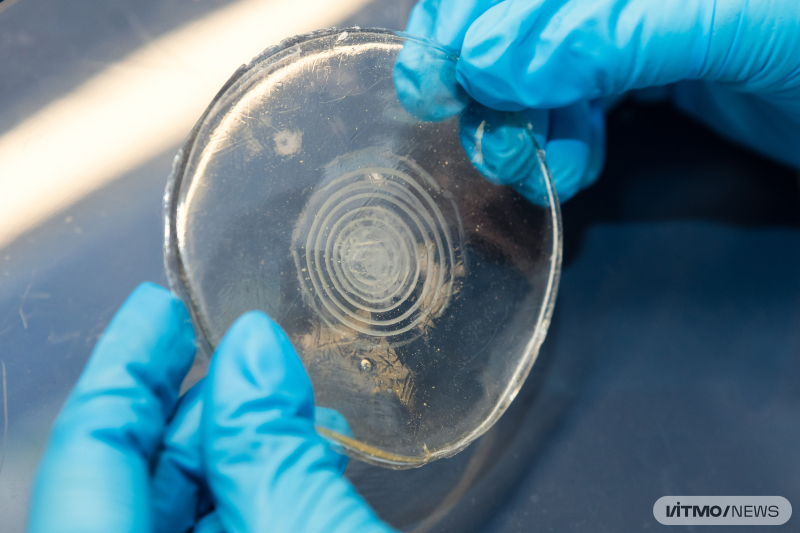
«В основе нашей системы — гидроксиапатит (минерал, формирующий костную ткань). Решение представляет собой несколько колец Лизеганга — концентрических кругов, образованных при осаждении раствора. Преимущественно на этих кольцах мы вырастили клетки. Один из вариантов передачи сигнала между ними происходит через ионные каналы. Мы добавили активатор работы кальциевых каналов (норэпинефрин), чтобы с его помощью оценить особенности распределения сигнала по кольцам и между ними. Второй компонент системы — гибкие ион-селективные электроды. Их мы использовали для изменения возникающих ионных токов. Волнообразное перераспределение сигнала после активации ионных каналов доказывает передачу сигнала между клетками», — отметила Полина Зырянова, первый автор исследования и инженер научно-образовательного центра инфохимии ИТМО.
Полина Зырянова. Фото из личного архива автора
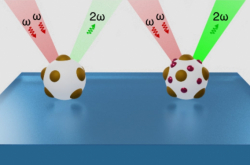
Как отметили авторы проекта, связь между кольцами напоминает сообщение между городами. Клетки обособленно располагаются на кольцах, но при этом «чувствуют» друг друга на расстоянии, то есть могут передавать сигналы и расти навстречу, хотя у них нет органов чувств или разума. Также при разработке платформы для клеточной коммуникации они обнаружили, что наиболее интенсивный рост клеток возникал на третьем кольце гидроксиапатита — там же был максимальный пьезоэлектрический эффект. Он играет важную роль в регенерации костной ткани — трансформирует механическое давление в электрические импульсы, которые привлекают стволовые клетки. Они развиваются в остеобласты и формируют новую костную ткань или делают существующую более плотной.
Например, если человек занимается боевыми искусствами, кости его ног со временем становятся более прочными, чем у неспортсмена. Такое отличие возникает как раз из-за постоянного механического давления и возникающего пьезоэффекта. Изучение влияния пьезоэффекта на межклеточное взаимодействие поможет создать функциональные материалы для системы таргетной доставки лекарств.
«Мы предложили модельную биомиметическую систему, похожую по своим свойствам на настоящую кость с пьезоэффектом. Дополнительно в нее можно внедрить вещества, которые помогут клеткам быстрее расти или высвобождать лекарства. Эти результаты могут быть полезны в разработке способствующих ускоренной клеточной регенерации имплантатов. Мы планируем продолжить исследования по восстановлению нарушенной клеточной коммуникации, наша цель — создать материал, который клетки будут принимать за “своих”», — рассказала Светлана Уласевич, один из авторов исследования и доцент научно-образовательного центра инфохимии ИТМО.
Светлана Уласевич. Фото: Дмитрий Григорьев / ITMO.NEWS
Исследование поддержано Российским научным фондом (грант №21-13-00403 и №19-79-10244).