Фибрилляция предсердий — одна из самых распространенных аритмий, которая поражает до 2% населения. Это патологическое состояние, при котором разрастается соединительная ткань и появляются рубцовые изменения — как правило, в результате хронического воспаления. Из-за этого сердечный ритм больного учащается и становится нерегулярным — обычно он достигает больше 400 ударов в минуту. Болезнь может привести к образованию тромбов в сердце, а также увеличивает риск инсульта, сердечной недостаточности и других осложнений.
Чтобы снизить риски развития опасных состояний при фибрилляции предсердий, пациентам назначают антиаритмики, антикоагулянты и другие препараты. Но и они не всегда справляются с симптомами — в таком случае врач может порекомендовать хирургическое лечение, в частности, катетерную абляцию. Это операция, при которой в сердце вводят катетер, чтобы изолировать легочную вену и разрушить участки ткани, вызывающие аномальное сердцебиение.
При этом даже после катетерной абляции болезнь может вернуться — рецидив случается в 20–45% случаев, и операцию приходится делать снова. Это происходит потому, что в стандартном протоколе проведения операции нет предсказательной системы, которая могла бы оценивать эффективность наносимого «шрама».
Сделать операцию более эффективной можно, если проводить ее по индивидуальному протоколу, который учитывает особенности конкретного пациента: строение сердца, разрастание ткани и другие.
Сейчас в мире существует единственная система, которая позволяет составлять индивидуальный протокол для проведения катетерной абляции, — OPTIMA, разработанная в университете Джонса Хопкинса. На основе МРТ она создает трехмерную симуляцию сердца и позволяет предсказать результат операции. Сегодня OPTIMA снижает риски рецидивов на 30%.
По словам PI Лаборатории экспериментальной и компьютерной кардиологии Передовой инженерной школы (ПИШ) ИТМО Валерии Цвелой, проблема этой системы в том, что в ее основе лежит электрофизиологическая модель. Такая модель не учитывает морфологические особенности клеток сердца: форму, размер и другие параметры, которые сильно влияют на условия возникновения аритмии, а значит и на форму «шрама».
Что сделали в ИТМО
Чтобы предотвратить негативные последствия операции, ученые Передовой инженерной школы ИТМО совместно с коллегами из Альметьевского государственного нефтяного института, ПАО «Татнефть», МФТИ, Московского областного научно-исследовательского клинического института имени М.Ф. Владимирского и Клинической больницы №1 Управления делами Президента РФ предложили подход, который позволит составить индивидуальный протокол операции под конкретного пациента с помощью имитационного моделирования. На основании МРТ-снимков сердца нейросеть реконструирует предсердную проводимость, то есть находит нарушения сердечного ритма. Ученые предполагают, что предложенная модель позволит снизить вероятность рецидивов более чем на 30%.
Подход основан на клеточной модели, которая для создания протокола операции ищет фиброз — области с фибробластами, или клетками, которые не проводят импульс в сердце и затрудняют его нормальную работу. Ученые предполагают, что клеточная модель будет потенциально более чувствительной к индивидуальным данным по фиброзу пациента, чем обычная электрофизиологическая. Этот подход более персонализированный, так как фиброз у каждого пациента свой и операция пройдет эффективнее, если учитывать индивидуальные особенности.
Подход включает в себя три этапа. На первом нейросеть сегментирует МРТ-данные и определяет строение предсердий — в соответствии с этим алгоритм описывает, какие клетки фиброзные, а какие — здоровые. Алгоритм распределяет клетки по картине фиброза в соответствии с методом параметризации и создает электронный дубликат сердца. Затем нейросеть моделирует оптимальные протоколы проведения операции — врачи cмогут рассмотреть несколько вариантов и выбрать наиболее подходящий. Источник: AIP Publishing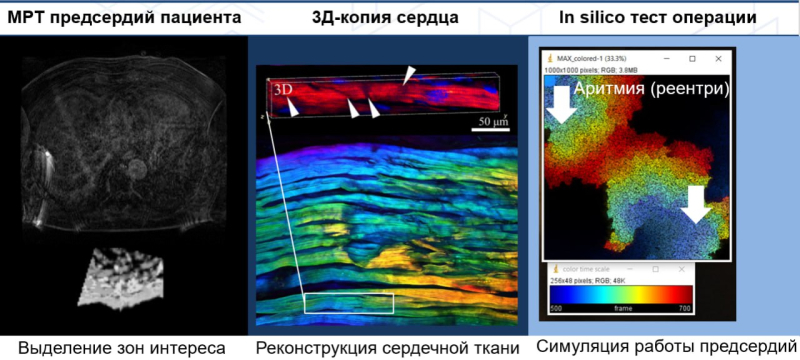
Чтобы обучить модель, специалисты использовали около 70 МРТ-снимков сердца (это более 300 изображений в разных плоскостях) до и после катетерной абляции из открытых источников.
Что дальше
Ученые уже создали прототип нейронной сети для сегментации стенок предсердий и фиброза и планируют продолжить работу над системой. Предложенный метод позволит создать систему поддержки принятия решений для кардиохирургов — для этого нужно получить больше размеченных МРТ-снимков. Система будет подсказывать врачам оптимальный для конкретного пациента протокол операции, при котором аритмия вернется с меньшей вероятностью.
«Мы уже определили параметры для клеток, которые помогут составить клеточную модель, собрали часть данных по биоэлектрическим потенциалам клеток пациентов разных возрастов, начали обучать алгоритмы работать с этими данными и сделали тестовый вариант нейросети, которая умеет по снимкам МРТ определять форму предсердий и фиброзных образований в них. В дальнейшем мы планируем объединить все наработки в одну систему: собрать больше данных по разным пациентам, дообучить алгоритмы, привести их в единую программу и пройти несколько этапов сравнений с существующими аналогами», — рассказала руководительница проекта, PI Лаборатории экспериментальной и компьютерной кардиологии ПИШ ИТМО и АГНИ Валерия Цвелая.